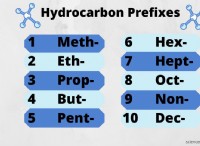
化学は物質の研究であり、日常の活動で物質が受ける変化を研究します。本質的に、化学の中心には、世界中の変化を研究することが含まれます。原子、分子、そしてそれらが作る物質、つまり元素と化合物のいくつかの基本的な考え方について議論しましょう。元素と化合物の特性は、それらの構造によって決定されます。コンポーネントの唯一の構造単位は原子です。原子はとても小さいです。
原子の構造
原子には、陽子、電子、中性子の 3 つの基本的な粒子が含まれています。原子の核(中心)には陽子(正電荷)が含まれているため、中性子(電荷なし)が含まれています。原子の最も外側の領域は電子殻と呼ばれ、電子(負に帯電)を含んでいます。原子には、基本的な粒子の配置と数をサポートするさまざまなプロパティがあります。原子(H)には陽子が 1 つと電子が 1 つだけ含まれており、中性子は含まれていません。これは、番号を使用して決定され、したがって要素の質量数になります。
- 原子番号- コンポーネントの数は、その原子核内に存在する陽子の数に十分です。例:水素には 6 つの陽子があり、酸素には 8 つの陽子があります。
- 質量数- 核子数は、原子核内に存在するさまざまな陽子と中性子の合計です。 A で示されます
A =Z+n
Z は陽子の数です
N は中性子の数です。
例:炭素には 6 個の陽子と 6 個の中性子があります。原子量は 12 です。水素には 1 個の陽子と 0 個の中性子がありますが、原子量は 1 です。
ダルトンの原子理論
ダルトンは、空気中の気体の挙動を研究しました。彼は、化合物内の要素が常に同じように起こる理由を解明する理論を開発しました。ダルトンは、個々の物質は分割できない原子と呼ばれる個々の粒子から形成されているという考えを提案しました。すべての元素は原子で構成されています。同じ元素の原子はすべて同じ質量を持ち、さまざまな元素の原子は異なる質量を持ちます。化合物には、複数の元素の原子が含まれています。特定の化合物の間に、さまざまな元素の原子が常に同じように結合します。
原子と分子の間の力
分子間力(IMF)(または二次力)は、分子間の相互作用を媒介する力です。これには、原子と他の種類の隣接粒子との間に作用する引力または反発の電磁力が含まれます。原子またはイオン。分子間力は、分子内力(分子を一緒に保持する力)に比べて弱いです。たとえば、原子間で電子対を共有する化学結合は、隣接する分子間に存在する力よりもはるかに強力です。両方の力のセットは、分子力学で頻繁に利用される力場の重要な部分です。
分子間引力は次のタイプに分類されます。
- 水素結合
- イオン誘起双極子力
- イオン双極子力
- ヴァンダー ワールスの力
水素結合:1 つの分子の陽子と反対側の電気陰性原子との間の静電引力に起因する 2 つの分子間の弱い結合である可能性があります。
イオン誘起双極子力:原子または非極性分子内でイオンの接近によって双極子が誘起されるときに生じる弱い引力である可能性があります。
イオン双極子力:イオン双極子力は、イオンと双極子を特徴とする中性分子との間の静電引力 から生じる引力です。
ファン デル ワールス力:中性分子を液体と固体全体で少なくとも 1 つに引き寄せる比較的弱い電気力である可能性があります。
元素と化合物の化学結合の法則:
化学結合の法則は、2 つの元素が結合して完全に 1 つの化合物を形成する場合、別の元素の固定質量と混合する 1 つの元素の質量が小さな整数の比率内にあることを示しています。
<オール>結論:
宇宙内のすべての物質は、純粋な元素、結合した化合物、または原子と化合物の混合物で構成されています。すべての要素は原子で構成されています。原子にはさまざまな質量と組織があります。電子、陽子、中性子が原子を作ります。 2 つの原子が結合すると、分子が形成されます。