主な違い - 反応速度と速度定数
化学反応には、基本的に生成物と反応物が含まれます。それとは別に、化学反応が完了するまでに必要ないくつかの重要な条件があります。これらの条件には、適切な温度と圧力、イオン強度などが含まれます。ただし、すべての化学反応は、反応速度と速度定数という 2 つの用語を使用して説明できます。反応速度は反応が進行する速度を表し、速度定数は反応速度を定量化します。反応速度と速度定数の主な違いは、反応速度は単位時間あたりの反応物の濃度の変化または生成物の濃度の変化です。 速度定数は、特定の反応速度に関連する比例定数です。
対象となる主な分野
1.反応率とは
– 定義、プロパティ、例
2.レート定数とは
– 定義、プロパティ、例
3.反応速度と速度定数の違いは何ですか
– 主な違いの比較
重要な用語:イオン強度、生成物、速度定数、反応速度、反応物

反応率とは
反応速度または反応速度は、単位時間あたりの反応物の濃度の変化または生成物の濃度の変化です。これは、2 つの方法で取得できます。 1 つは、反応中に消費された反応物の濃度を、その消費に要した時間で割ることです。もう 1 つの方法は、反応の最後に形成された生成物の濃度を、その形成に要した時間で割ることです。これは以下のように短縮できます。
レート =[濃度] / 時間
しかし、ほとんどの場合、すべての反応物が反応のために消費されるわけではありません。したがって、成分の濃度は、特定の時間における「濃度の変化」と見なされます。これは記号 Δ で与えられます。時刻が t1 のときに濃度を測定した場合 そして t2 の場合、反応にかかる時間は (t2 -t1 ) =経過時間 (Δt)。したがって、時間は Δt と見なされます。その後、反応が完了する前でも反応速度を測定できます。
レート =Δ[反応物] / Δ 時間 =Δ[製品] / Δ 時間
生成物 C を与える A と B の間の反応を考えてみましょう。
A + B → C
上記の反応の場合、A、B、または C の濃度変化を測定することで反応速度を測定できます。
レート =– Δ [A] / Δt
レート =– Δ [B] / Δt
レート =Δ[C] / Δt
A と B の濃度の前にマイナス記号があることに注意してください。これは、Δt の期間中の反応物の減少を示すために使用されます。ただし、C 濃度の前にマイナス記号はありません。これは、C が消費されるのではなく生成されるため、C 濃度が反応全体で増加するためです。
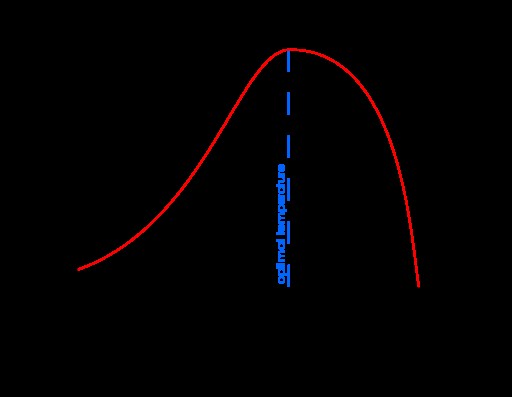
図 1:反応速度と温度のグラフ
上のグラフは、酵素反応の温度に対する反応速度の依存性を示しています。最適温度は、反応速度がピークに達する温度です。
レート定数とは
速度定数は、特定の反応速度に関連する比例定数です。システムの温度に依存します。速度定数は、反応速度についてのアイデアを提供します。速度定数の記号は「k」です。たとえば、生成物 C を生成する A と B の間の反応の場合、
率 =– Δ [A] / Δt
∴ 率 α [A]
率 =– Δ [B] / Δt
∴ レート α [B]
上記の関係を使用して、以下のように反応速度の方程式を作成できます。
レート =k[A][B]
ここで、
k は速度定数です。
[A] は A の濃度 [B] は B の濃度a は A に関する反応の順序です
b は B
に関する反応の順序です。特定の温度では、速度定数は温度の変化に応じて変化する明確な値を持ちます。この温度依存性は、「アレニウスの式」と呼ばれる式で与えられます。
K =Ae
ここで、
K は速度定数です
A は前指数因子です
EA は反応の活性化エネルギーです
R は普遍気体定数です
T はシステムの温度です
この方程式は、速度定数に対する温度変化の影響と触媒の影響を示しています。温度を上げると、速度定数が増加します。反応混合物に触媒を添加すると、活性化エネルギーが減少し、速度定数が増加します。
反応速度と速度定数の違い
定義
反応率: 反応速度は、単位時間あたりの反応物の濃度の変化または生成物の濃度の変化です。
速度定数: 速度定数は、特定の反応速度に関連する比例定数です。
モル濃度
反応率: 反応速度は、反応物と生成物のモル濃度に依存します。
レート定数: 速度定数は、反応物と生成物のモル濃度に依存しません。
気温
反応率: 反応速度は温度に間接的に依存します。
レート定数: 速度定数は基本的に温度に依存します。
時間
反応率: 反応速度は、反応にかかる時間によって異なります。
レート定数: 速度定数は、反応にかかる時間には依存しません。
結論
特定の化学反応に最適な条件 (温度など) を決定するには、反応速度と速度定数が非常に重要です。そうすれば、反応の取り扱いが容易になり、短時間で最適な量の生成物を得ることができます。したがって、特性と、反応速度と速度定数の違いを理解することは非常に重要です。







