主な違い – 無機酸と有機酸
酸は、酸性の性質を持つ化合物です。酸は、塩基と反応して塩と水を形成する化学種として定義することもできます。酸には主に強酸と弱酸の 2 種類があります。酸は、化学組成に応じて鉱酸と有機酸に分類することもできます。鉱酸と有機酸の主な違いは、鉱酸はさまざまな化学元素の組み合わせで構成される無機化合物であるのに対し、有機酸は本質的に炭素原子と水素原子で構成される有機化合物です。
対象となる主な分野
1.ミネラル酸とは
– 定義、プロパティ、例
2.有機酸とは
– 定義、プロパティ
3.無機酸と有機酸の類似点は何ですか
– 共通機能の概要
4.ミネラル酸と有機酸の違いは何ですか
– 主な相違点の比較
重要な用語:酸、炭素、共役塩基、腐食性物質、無機酸、鉱酸、有機酸
ミネラル酸とは
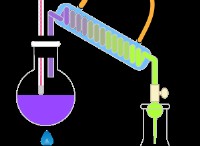
鉱酸または無機酸は、無機化合物に由来する酸です。したがって、無機酸は酸性の性質を持つ無機化合物です。一部の無機酸には構造内に酸素原子が含まれていますが、一部の無機酸には含まれていません。たとえば、H2 SO4 酸素原子を持つ無機酸です。しかし、別の無機酸である HCN には酸素原子がありません。
無機酸には炭素原子を含むものもあれば、化学構造に炭素を含まない無機酸もあります (無機酸とは異なり、有機酸は必ず炭素で構成されます)。例えば、HCNは無機酸ですが、炭素原子を持っています。 HCN は、有機化合物とは異なり、水中では C-H 結合のみが容易に H イオンと CN イオンに解離するため、有機酸ではありません。

図 1:硝酸発煙
鉱酸は水溶性が高く、有機溶媒には溶けません。ほとんどの鉱酸は非常に腐食性があります。最も一般的な鉱酸は、硫酸、塩酸、および硝酸です。鉱酸には、有機化合物と無機化合物の両方の合成を含む多くの用途があります。ただし、これらの酸は非常に腐食性があります。
有機酸とは
有機酸は、酸性の性質を持つ有機化合物です。これらは有機化合物であるため、有機酸は構造内に炭素原子を持っている必要があります。最も一般的なタイプの有機酸はカルボン酸です。カルボン酸の分子式は、RCOOHで表すことができます。酸性の原因となる官能基は-COOHです。このグループの水素原子は、H イオンとして放出できます。これは、酸素原子が電子に富み、H 原子よりも電気陰性度が高いためです。したがって、この H 原子は –COOH 基から簡単に分離できます。
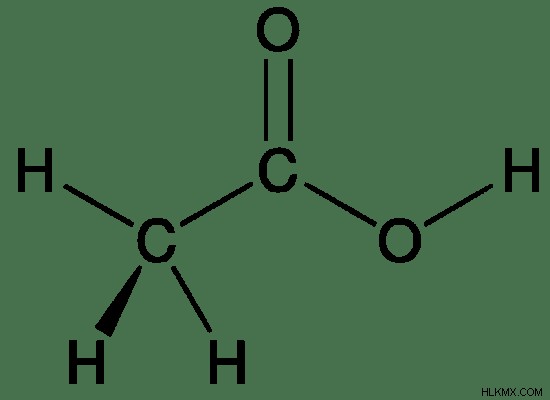
図 2:酢酸は有機酸です
酸性の特性により、有機酸は 7 未満の pH 値を示します。これらの酸は青リトマス赤に変わり、酸味があります。有機酸には 2 種類あります。
- 強い有機酸
- 弱有機酸
弱酸は、溶液中で共役塩基および H イオンと平衡状態で存在しますが、強酸は完全に解離しており、水溶液中で平衡状態にありません。ほとんどの有機酸は、水中で部分的に解離するため、弱酸 (例:エタン酸) です。しかし、ほとんどすべての有機酸は有機溶媒に溶解しています。解離後に形成される陰イオンの安定性により、有機酸は強酸または弱酸になります。
鉱酸と有機酸の類似点
- どちらの物質も酸性の性質を持っています
- どちらのタイプも陽子 (H イオン) を放出できます
- どちらも塩基と反応できます
- どちらのタイプも青リトマス赤に変わります。
- どちらのタイプにも強酸と弱酸があります。
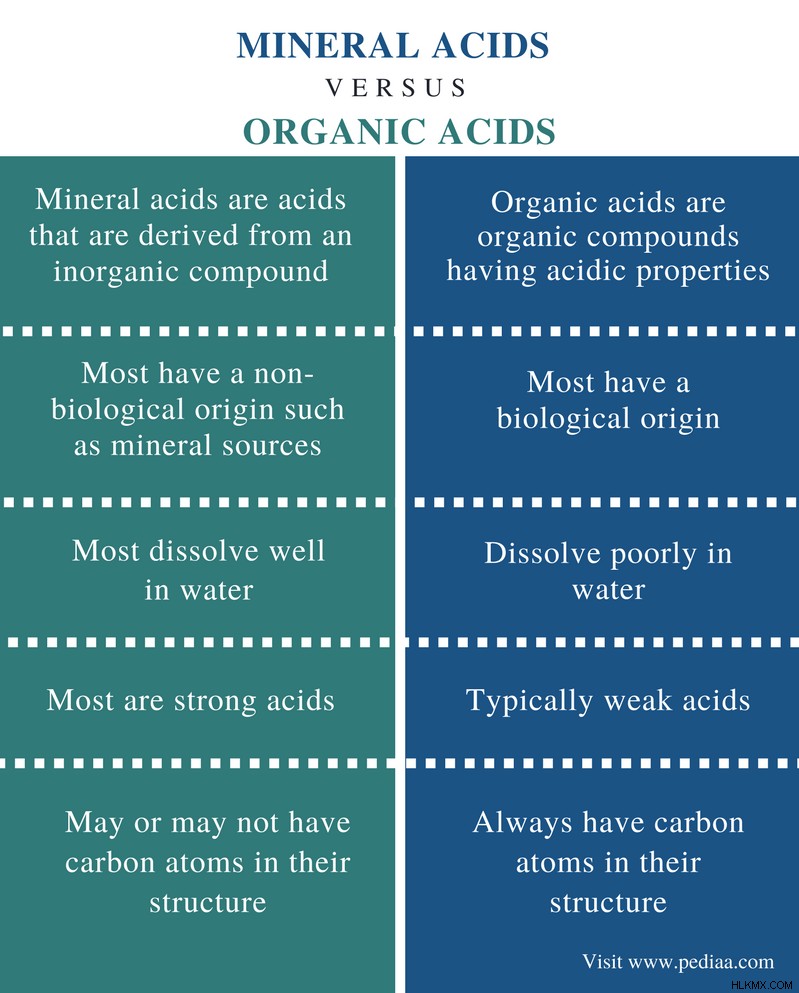
ミネラル酸と有機酸の違い
定義
ミネラル酸: 鉱酸または無機酸は、無機化合物に由来する酸です。
有機酸: 有機酸は、酸性の性質を持つ有機化合物です。
起源
ミネラル酸: ほとんどの鉱酸は、ミネラル源などの非生物学的起源を持っています.
有機酸: ほとんどの有機酸は生物由来です。
溶解度
ミネラル酸: ほとんどの鉱酸は水によく溶けます。
有機酸: 有機酸は水に溶けにくい。
酸度
ミネラル酸: ほとんどの鉱酸は強酸です。
有機酸: 有機酸は通常、弱酸です。
化学組成
ミネラル酸: 鉱酸は、その構造に炭素原子を含む場合と含まない場合があります。
有機酸: 有機酸は基本的にその構造に炭素原子を持っています。
結論
酸は、有機酸と無機酸に分類できます。鉱酸は無機酸としても知られています。鉱酸と有機酸の主な違いは、鉱酸はさまざまな化学元素の組み合わせで構成される無機化合物であるのに対し、有機酸は本質的に炭素原子と水素原子で構成される有機化合物であるということです.