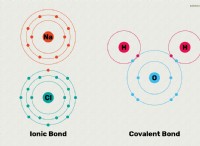
a ラジカル 対立する電子を持つ原子または原子のグループです。これにより、ラジカルは他の分子と簡単に反応して新しい結合を形成できるため、非常に反応性が高くなります。分子が熱または光にさらされるときなど、化学結合が壊れているときにラジカルが形成されることがよくあります。
A 分子 一方、化学結合によって結合された原子のグループです。分子は任意の数の原子で構成することができ、それらは充電または中性のいずれかです。分子は物質の基本的な構成要素であり、私たちの周りに見られるすべてを構成しています。
ここにラジカルと分子の重要な違いを要約するテーブルがあります:
|機能|ラジカル|分子|
| --- | --- | --- |
|対応のない電子の数|少なくとも1つ|なし|
|反応性|反応性|反応性が低い|
|フォーメーション|化学結合が壊れたときに形成されます|化学結合が形成されたときに形成されます|
|例|水素原子、ヒドロキシルラジカル|水分子、二酸化炭素分子|
結論
ラジカルと分子はどちらも化学の重要な概念です。ラジカルは非常に反応性があり、他の分子と簡単に反応して新しい結合を形成することができますが、分子は物質の基本的な構成要素です。ラジカルと分子の違いを理解することにより、化学反応がどのように機能し、私たちの周りの世界がどのように構成されているかをよりよく理解することができます。