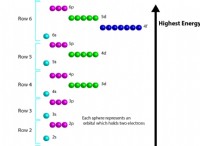
原子の電子構造は、その化学的性質と放出スペクトルを決定します。原子の発光スペクトルは、電子がより高いエネルギーレベルに励起され、元のエネルギーレベルに戻ると、原子が放出する光の波長のユニークなパターンです。
電子構造が色をどのように説明するか
異なる要素は、異なる電子構造を持っているため、異なる色の光を放出します。原子電子のエネルギーレベルは、核内の陽子の数と原子の電子の数によって決定されます。電子がより高いエネルギーレベルに励起されると、2つのエネルギーレベルの差と同じエネルギーの光の光子を吸収します。電子が元のエネルギーレベルに戻ると、同じ量のエネルギーで光の光子を放出します。
光の光子の波長は、そのエネルギーに反比例します。これは、波長が短い光子には、波長が長い光子よりもエネルギーが多いことを意味します。可視スペクトルの色は、赤(最長波長)からバイオレット(最短波長)に配置されています。
異なる要素は、異なる電子構造を持っているため、異なる色の光を放出します。これは、電子のエネルギーレベルが異なり、異なる波長で光の光子を吸収して放出することを意味します。
電子構造と色の例
電子構造がさまざまな花火の色をどのように説明しているかの例をいくつか紹介します。
* ナトリウム 原子は、熱電子が加熱されると、より高いエネルギーレベルに興奮するため、黄色オレンジ色の光を放出します。このエネルギーレベルは、元のエネルギーレベルから約2.1電子ボルト(EV)です。電子が元のエネルギーレベルに戻ると、目に見えるスペクトルの黄色のオレンジ色の部分にある波長の光子を発します。
* 銅 原子は、熱が加熱されると、電子がより高いエネルギーレベルに興奮するため、緑色の光を放出します。このエネルギーレベルは、元のエネルギーレベルよりも約2.9 eVです。電子が元のエネルギーレベルに戻ると、目に見えるスペクトルの緑色の緑色の波長で光の光子を放出します。
* strontium 原子は、熱が加熱されると、電子がより高いエネルギーレベルに興奮するため、赤色光を放出します。このエネルギーレベルは、元のエネルギーレベルよりも約1.8 eVです。電子が元のエネルギーレベルに戻ると、目に見えるスペクトルの赤い部分にある波長が約688 nmの光の光子を放出します。
結論
原子の電子構造は、その発光スペクトルとその色を決定します。これが、異なる要素が加熱または励起されるときに異なる色の光を放出する理由です。この知識は、さまざまな美しい色を生成する花火を作成するために使用されます。