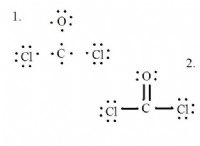ナトリウムは高度に反応性のある金属であり、その価電子を容易に失い、正の帯電イオン(Na+)を形成します。一方、硫黄は、外側のシェルを完成させるために電子を獲得する傾向がある非金属です。これらの2つの要素が一緒になると、ナトリウムが電子を失う傾向は、硫黄の電子を獲得する傾向とよく一致します。これにより、イオン化合物である硫化ナトリウム(Na2S)の形成が生じ、そこではナトリウム原子が硫黄原子に伝達され、正に帯電したナトリウムイオン(Na+)と負に帯電した硫化物イオン(S2-)が生成されます。これらの反対に帯電したイオン間の静電引力は、化合物をイオン格子で一緒に保持します。