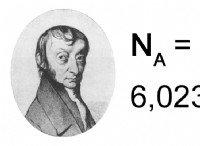同位体の理解
* 同位体 同じ元素の原子(同じ数の陽子)ですが、中性子の数は異なります。
* 原子番号: プロトンの数は要素を定義します。この場合、11の陽子は元素がナトリウム(NA)であることを意味します。
* 質量数: 質量数は、陽子と中性子の合計です。
ナトリウム(Na)の可能性のある同位体
* 元の原子: この原子には質量数が24(11陽子 + 13個の中性子)があります。 ナトリウム-24(²⁴NA)として表現できます
* 他の可能な同位体: プロトンの数はナトリウムであるために同じままでなければならないため、変化させることができるのは中性子の数だけです。 ここにいくつかの例があります:
* ナトリウム-22(²²NA): この同位体には11の陽子と11の中性子があります。
* ナトリウム-23(²³na): この同位体には11個の陽子と12個の中性子があります。
* ナトリウム-25(²⁵NA): この同位体には11の陽子と14の中性子があります。
* ナトリウム-26(²⁶NA): この同位体には11の陽子と15の中性子があります。
重要な注意: すべての同位体が等しく安定しているわけではありません。ナトリウム-23は、ナトリウムの最も一般的で安定した同位体です。ナトリウム24やナトリウム-26などの一部の同位体は放射性です。