* 分子運動: ガス分子は常にランダムな動きで、互いに衝突し、容器の壁が衝突します。この動きは運動エネルギーと呼ばれます 。
* 温度と運動エネルギー: ガスの温度が高いほど、分子が速く移動し、平均運動エネルギーが大きくなります。逆に、温度が低くなると、分子運動が遅くなり、平均運動エネルギーが低くなります。
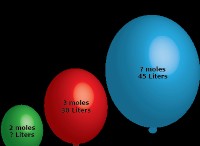
* 直接比例: 温度と運動エネルギーの関係は直接比例します。これは、ガスの温度を2倍にすると、分子の平均運動エネルギーを2倍にすることを意味します。
これが類推です: 踊る人々のグループを想像してみてください。それらがすべてゆっくりと落ち着いて動いている場合、ダンスフロアの「温度」は低いです。彼らが乱暴かつエネルギー的に踊り始めると、ダンスフロアの「温度」が増加します。
キーポイント:
* 平均運動エネルギー: 温度は分子の *平均 *運動エネルギーの尺度であり、個々の分子の速度にいくらかの変動があることを意味します。
* 絶対温度: ケルビン(k)で測定された絶対温度スケールは、運動エネルギーに直接関係しています。ゼロケルビン(0 k)は絶対ゼロであり、分子運動が理論的に停止します。
* 内部エネルギー: ガス内のすべての分子の総運動エネルギーは、その内部エネルギーに寄与します。
アプリケーション:
* ガス法: ガスの温度、圧力、および体積(理想的なガス法)の関係は、その分子の運動エネルギーに基づいています。
* 熱力学: 熱とエネルギーの移動の研究は、温度が分子運動にどのように関連するかを理解することに大きく依存しています。
* 化学: 化学反応は、分子が衝突して反応する速度に影響を与えるため、温度の影響を受けることがよくあります。
さらに質問がある場合はお知らせください!