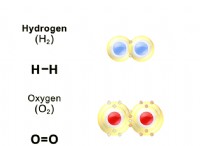
1。酸素の電子構成: 酸素には外側のシェルに6つの電子があり、オクテットを完成させるにはさらに2つの電子が必要です。 2つの水素原子と2つの共有結合を形成することにより、これを達成します。
2。電子の孤立ペア: 酸素には、外殻に2つの孤立した電子のペアがあります。これらの唯一のペアは、電子の結合ペアを撃退し、2つの水素原子を近くに押します。
3。 vSEPR理論: 価数シェル電子ペア反発(VSEPR)理論は、中心原子の周りの電子ペアが反発を最小限に抑えるために自分自身を整えると述べています。酸素の2つの孤立ペアは、結合ペアよりも強い反発力を発揮し、水素原子を押し下げ、形を曲げます。
4。ハイブリダイゼーション: 酸素の原子軌道はハイブリダイズして、4つのSP3ハイブリッド軌道を形成します。これらの軌道のうち2つは水素原子と共有結合を形成し、他の2つの軌道は孤立ペアで占められています。このハイブリダイゼーションは、曲がった形にさらに寄与します。
要約: 水の形状は、酸素の電子構成、孤立ペア反発、およびVSEPR理論の組み合わせの結果です。 この曲がった形状は、極性や水素結合を形成する能力など、多くのユニークな特性を水に与えます。