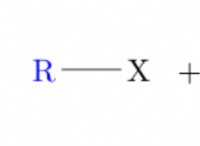* 電子構成: 基底状態の炭素には、電子構成1S²2S²2p²があります。安定したアニオンを形成するために、それは余分な電子を獲得し、その構成1S²2S²2P³になります。これは、2p軌道に3つの対応のない電子があることを意味します。
* ハイブリダイゼーション: SP2ハイブリダイゼーションの場合、1つのS軌道と2つのp軌道を混合する必要があります。炭素陰イオンには、p軌道に3つの対応のない電子があり、S軌道には1つの対応のない電子のみがあります。結合に関与するすべての電子に対応するためのハイブリダイゼーションは必要ありません。
* 結合: 炭素陰イオンは4つの単一結合を形成し、四面体の幾何学に向けられています。この四面体の形状は、SP3ハイブリダイゼーションで最もよく説明されます。ここでは、1つの軌道と3つのp軌道が混合して4つのSP3ハイブリッド軌道を作成します。
要約:
*炭素陰イオンはSP2ハイブリダイゼーションを示しません。
*彼らは、SP3ハイブリダイゼーションを好み、四面体の幾何学に4つのSigma結合を形成します。
* Carbonの電子構成に追加の電子を追加すると、その結合挙動とハイブリダイゼーションの必要性が変わります。