1。臭素の特性を理解する:
* 価電子: 臭素(BR)には、7つの価電子(最も外側の殻の電子)があります。
* 安定性: 原子は、安定性のために電子の完全な外殻(ほとんどの原子で8)を持っていることを求めています。
2。結合プロセス:
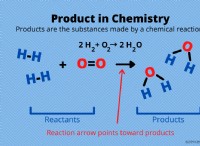
* 電子の共有: 安定した構成を実現するために、2つの臭素原子がそれぞれ1つの電子を共有します。この共有電子のペアは、共有結合を形成します。
* 分子軌道形成: 2つの原子軌道(各臭素原子からの1つ)が重複すると、それらは新しい低エネルギー分子軌道を形成します。共有電子はこの分子軌道を占有し、より強力でより安定した配置をもたらします。
* 非極性共有結合: 両方の臭素原子は同じ電気陰性度(電子を引き付ける能力)と同じであるため、共有電子はそれらの間に等しく分布しています。これにより、結合は非極性になります。
3。視覚表現:
* ルイス構造: 結合は、2つの臭素シンボルを結ぶ単一の線で表されます。
`` `
BR -BR
`` `
* 電子ドット図: これは、原子価電子と共有ペアを示しています。
`` `
:br。 .br:
| |
| |
| |
:br。 .br:
`` `
要約: 2つの臭素原子間の共有結合は、一対の電子を共有することにより形成され、非極性共有結合を持つ安定した分子をもたらします。