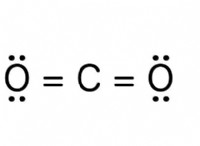説明:
* 水素結合: 水分子は、強い分子間力である水素結合を形成することができます。酸素は非常に電気陰性であり、酸素原子に部分的な負電荷と水素原子に部分的な正電荷を生成します。これにより、水分子は強力な双極子型相互作用と水素結合を形成できます。
* メタン(CH4): メタン分子は非極性であり、最も弱いタイプの分子間力であるロンドン分散力が弱いだけです。
したがって、水中のより強力な水素結合は、メタン中のロンドン分散力の弱い力と比較して、分子間の魅力的な力が大幅に高くなります。
キーポイント:
*分子間力が強くなると、より高い沸点、融点、および表面張力が発生します。
*水は、メタン(-161°C)よりも高い沸点(100°C)を持っており、水分子間のより強い引力の力を反映しています。