その理由は次のとおりです。
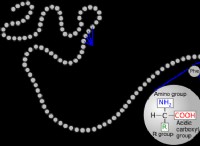
* 極性: 極性分子は電荷の分離を持ち、正と負の端を生み出します。水は素晴らしい例であり、その酸素原子はわずかに陰性であり、その水素原子はわずかに陽性です。
* 塩と砂糖: 塩(NaCl)と砂糖(スクロース)の両方は極です 分子。塩はイオン化合物であり、陽性ナトリウムイオン(Na+)と負の塩化物イオン(CL-)の間に強い静電魅力を形成します。砂糖には、多くの極性ヒドロキシル基(-OH)を持つ複雑な構造があり、これも引力を生み出します。
* 灯油: 灯油は非極性です 炭化水素。炭素と水素の原子の長い鎖で作られており、電荷の有意な分離はありません。
ルール: 「ように解散するように。」これは、極性物質が他の極性物質に最も溶解することを意味し、非極性物質は非極性物質に最も溶解することを意味します。
それが機能しない理由: 極性塩と糖分子の間の強い引力は、非極性灯油分子と形成される可能性のある弱い相互作用よりもはるかに強いです。 したがって、それらはバラバラになり、灯油内で分散することはできません。
対照的に: 水は極性溶媒であるため、塩と砂糖が容易に溶けます。水分子は、塩分および糖分子の帯電した部分または極地と相互作用し、効果的にそれらを引き離し、水中に分散させることができます。