これがバランスの取れた化学式です:
ca(oh)₂(aq) + 2hno₂(aq)→ca(no₂)₂(aq) + 2h₂o(l)
説明:
* 水酸化カルシウム(Ca(OH)₂)は強いベースです。 水中で完全に解離し、水酸化物イオン(OH⁻)を放出します。
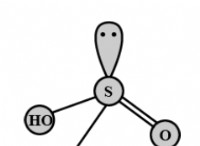
* 窒素酸(hno₂)は弱酸です。 水中で部分的に解離し、水素イオン(H⁺)を放出します。
* 中和反応: 塩基からの水酸化物イオンは、酸から水素イオンと反応して水を形成します(H₂O)。
* 亜硝酸カルシウム(Ca(no -)₂)は可溶性塩です。 それは水に溶け、溶液にとどまります。
重要なメモ:
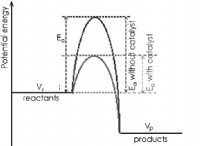
*反応は発熱性であり、熱を放出します。
*反応は通常、水溶液で実行されます。
*亜硝酸は不安定で、簡単に分解するため、新鮮なソリューションを使用することが重要です。
この反応は、酸塩基化学の典型的な例であり、中和反応の基本原理を実証しています。