1。 アトラクションと共有:
* 電気陰性度: 同様の電気陰性度(電子を引き付ける能力)の原子は、共有結合を形成する傾向があります。
* 価電子: 原子は、通常、電子の完全な外殻(貴族のような)を持つことにより、安定した電子構成を実現しようとします。彼らは電子を共有することによってこれを達成します。
2。 電子の共有:
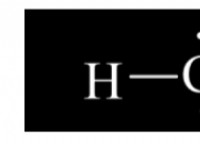
* 共有結合: 原子は原子価電子を共有して、両方の原子核に引き付けられる電子のペアを形成します。この共有ペアは、原子を一緒に保持する共有結合を作成します。
* 共有結合の種類:
* 単一結合: 1組の電子が原子間で共有されます。
* 二重結合: 2組の電子が共有されています。
* トリプルボンド: 3組の電子が共有されています。
3。 分子構造:
* 分子形状: 分子内の原子の配置は、その形状と特性を決定します。このジオメトリは、各原子の周りの電子ペア数とこれらの電子ペア間の反発の影響を受けます。
* 分子間力: 水素結合、双極子双極子力、ロンドン分散力などの分子間の弱いアトラクションは、分子化合物(融点、沸点など)の物理的特性に影響を与えます。
分子化合物の例:
* 水(h₂o): 2つの水素原子は、電子を酸素原子と共有し、2つの単一共有結合を形成します。
* 二酸化炭素(CO₂): 炭素は、2つの酸素原子を持つ2つの二重結合を共有します。
* メタン(Ch₄): 炭素は、4つの水素原子と単一の結合を共有しています。
分子化合物の重要な特性:
* 融点と沸点の低い: 共有結合は一般にイオン結合よりも弱いため、分子化合物は融点と沸点が低い傾向があります。
* 固体および液体状態の非導電性: 分子化合物は、電子が共有結合内に局在しているため、電気を導入しません。
* しばしば室温でのガスまたは液体: それらの弱い絆により、これらの州に存在することができます。
要約すると、原子が電子を共有して安定した電子構成を実現するときに分子化合物が形成されます。 この共有は、特徴的な特性を持つ特定の分子構造に原子を一緒に保持する共有結合を作成します。