その理由は次のとおりです。
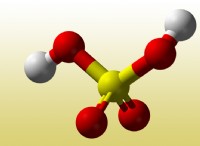
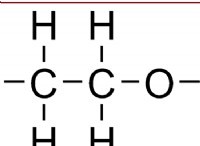
* 化学式: 化学式は、シンボルと式を使用して、化学反応に関与する反応物と生成物を表します。
* バランス: 方程式は、係数(化学式の前の数値)を調整してバランスが取れており、反応物側(左)の各要素の原子の数が、製品側のその要素の原子の数に等しいことを確認します。
例:
水素ガスと酸素ガス(O₂)と水を生成するための反応(H₂O)は、次のバランスの取れた方程式で表されます。
2h₂ +o₂→2h₂o
説明:
* 反応物: 2分子の水素ガス(H₂)と酸素ガスの1分子(O₂)
* 製品: 2つの水分分子(H₂O)
* バランス: 係数(2、1、および2)は、方程式の両側に4つの水素原子と2つの酸素原子があることを確認します。
このバランスは、化学反応では物質を作成または破壊することはできないと述べている質量の保全法則を反映しています。バランスの取れた方程式は、反応物の総質量が産物の総質量に等しいことを示しています。