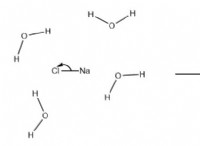
* 塩化水素(HCl): HClは共有化合物です 。これは、水素と塩素の原子が電子を共有して安定した結合を形成することを意味します。共有電子は、共有結合によって一緒に保持されている2つ以上の原子の離散単位である分子を作成します。
* 塩化ナトリウム(NaCl): NaClはイオン化合物です 。これは、ナトリウム(Na)が電子を失い、正の帯電イオン(Na+)になることを意味し、塩素(Cl)はその電子を負に帯電したイオン(CL-)に獲得します。 これらの反対に帯電したイオンは互いに静電的に引き付け、結晶格子を形成します 。 イオン化合物には離散分子はありません。これは、連続的で繰り返されるイオンです。
要約:
* 分子 原子が電子を共有する共有結合によって形成されます。
* イオン化合物 反対に帯電したイオン間の静電魅力によって形成され、離散分子を形成しないでください。
したがって、HClは分子と正しく呼ばれますが、NaClは正しく呼ばれません。