* 原子は通常中性です: 原子には、同数のプロトン(正の帯電した粒子)と電子(負に帯電した粒子)が含まれています。このバランスは中立電荷をもたらします。
* 電子の獲得: 原子が1つ以上の電子を獲得すると、負電荷の余剰を取得します。電子の数は現在、陽子の数を超えて、原子を負に帯電させます。
* イオン: 負に帯電した原子は、アニオンと呼ばれます 。
原子が電子を獲得する方法:
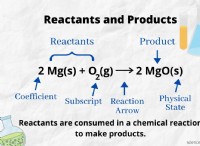
* 化学結合: 原子は、他の原子と化学結合を形成することにより電子を獲得できます。 たとえば、イオン結合では、ある原子は電子を失い、別の原子がそれを獲得します。
* 静電相互作用: 原子は、静電相互作用を通じて別の原子または分子から電子を獲得できます。これは、溶液や放射線にさらされた場合に発生する可能性があります。
例:
*塩素原子(CL)には17個のプロトンと17個の電子があります。
*電子を獲得して塩化物イオン(Cl-)を形成することができます。これには、現在17個のプロトンと18個の電子があります。
*この余分な電子は、塩化物イオンに負電荷を与えます。