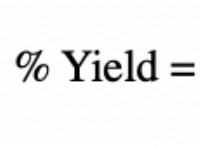* マグネシウムはアルミニウムよりも反応性が高い。 これは、マグネシウムが電子を失い、陽性イオンを形成する傾向が高いことを意味します。
* アルミニウムイオンが溶液中にあります。 これは、彼らがすでにイオンの形であることを意味します、al³⁺。
反応:
マグネシウム(Mg)は、その溶液からアルミニウム(AL)を変位させ、マグネシウムイオン(mg²⁺)と固体アルミニウム金属を形成します。
バランスの取れた化学式:
3mg(s) +2al³⁺(aq)→3mg²⁺(aq) + 2al(s)
あなたが観察するもの:
* バブル: マグネシウムと水との反応が水素を生成するため、水素ガス形成の泡を観察するかもしれません。
* 銀色の固体: 固体アルミニウム金属は溶液から沈殿し、銀色の固体を形成します。
* ソリューションは色を変えます: 溶液は、マグネシウムイオンが形成されると、無色または明るい色からより黄色がかった色に変化する可能性があります。
要約:
マグネシウムイオンとアルミニウムイオンの間の反応は、マグネシウムが酸化され(電子が失われる)、アルミニウムが減少する(電子を獲得)する酸化還元反応です。これにより、マグネシウムイオン、固体アルミニウム、およびおそらく水素ガスの形成が生じます。