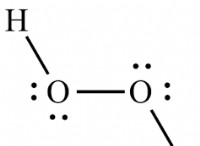
* ガソリンに溶解: ガソリンは非極性溶媒です。これは、ガソリンの分子が電子の比較的均等な分布を持っていることを意味し、その結果、分子の特定の部分で有意な陽性または負の電荷が得られません。
* 水に溶けない: 水は極性溶媒です。水分子は、正の端(水素原子の近く)と負の端(酸素原子の近く)を持っています。
結論:
物質Aは非極性溶媒(ガソリン)に溶解するが、極性溶媒(水)ではないため、物質Aは非極性でもあると結論付けることができます。 。
ここに:
* likeのように: 極性溶媒は極性溶質を溶解し、非極性溶媒は非極性溶質を溶解します。 分子構造の同様の性質により、相互作用して混合できます。
* 分子間力: 非極性分子は、弱いロンドン分散力によって結合されます。これらの力は、極性分子を一緒に保持する水素結合および双極子双極力の力よりもはるかに弱いです。
したがって、物質Aの分子は非常に可能性が高い:
* 非極性: これは、電子が分子内に均等に分布しているため、有意な陽性または負の電荷がないことを意味します。
* 分子間力が弱い: これは、非極性溶媒に溶解する能力と一致しています。