* 基本的な酸化物: これらは、酸と反応して塩と水を形成する酸化物です。それらは通常、金属によって形成されます。
* 可溶性: これは、酸化物が水に溶けることができることを意味します。
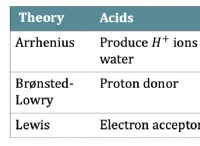
* ベース: ベースは、酸を中和できる物質です。
可溶性塩基性酸化物の例:
* 酸化ナトリウム(Na₂O): 水と反応して、強いアルカリである水酸化ナトリウム(NaOH)を形成します。
* 酸化カリウム(K₂O): 水と反応して、強いアルカリである水酸化カリウム(KOH)を形成します。
* 酸化カルシウム(CAO): 水と反応して、適度に強い基部である水酸化カルシウム(Ca(OH)₂)を形成します。
重要な特性:
* グループ1および2金属: 可溶性塩基性酸化物は通常、周期表のグループ1(アルカリ金属)およびグループ2(アルカリ地球金属)の金属によって形成されます。
* 高い反応性: これらの酸化物は水と非常に反応します。
* 水酸化物の形成: 可溶性塩基性酸化物の水との反応は、金属水酸化物を形成します。
化学式:
可溶性塩基性酸化物の水との一般的な反応は、次の方程式で表すことができます。
m₂o +h₂o→2moh
どこ:
* mは金属を表します
* MOHは金属水酸化物を表します
重要な注意: すべての金属酸化物が水に溶けるわけではありません。酸化鉄(III)のような不溶性(Fe₂O₃)もあります。