1。 要素の順序
* 一般的に: 低い電気陰性度を持つ要素が最初に記述されます。電気陰性度とは、原子が結合中に電子を引き付ける能力です。
* 例外:
* 水素(H) 常に最初にバイナリ化合物(2つの元素を持つ化合物)で書かれています。
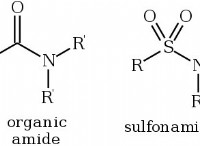
* 炭素(c) 通常、最初に有機分子(炭素を含む分子)で書かれています。
* 酸素(O) 通常、金属を含む化合物で最後に書かれています。
2。原子数のプレフィックス
* プレフィックスを使用 分子内の各タイプの原子の数を示すため。
* 一般的なプレフィックス:
* 1:モノ -
* 2:di-
* 3:Tri-
* 4:テトラ -
* 5:ペンタ -
* 6:ヘキサ -
* 7:hepta-
* 8:オクタ -
* 9:nona-
* 10:deca-
* 例: CO2は二酸化炭素(1つの炭素原子と2つの酸素原子)です。
3。式を簡素化
* 最初の要素のプレフィックスなしそれの原子が1つしかない場合。 たとえば、COは「一酸化モノカルボン」ではなく、一酸化炭素です。
* その要素の原子が1つしかない場合、2番目の要素からプレフィックス「モノ」をドロップします。 たとえば、SO2は「二酸化硫黄」ではなく二酸化硫黄です。
4。例外と共通名
*一部の共有化合物には、厳格な規則に従わない共通名があります(たとえば、水-H2O、アンモニア-NH3)。
*一部の化合物には、原子の数に応じて複数の式があります(たとえば、一酸化炭素 - CO、二酸化炭素-CO2)。
例:三酸化硫黄の式を書く
1。要素を識別します: 硫黄(S)と酸素(O)
2。各要素の数を決定します: 1つの硫黄原子と3つの酸素原子(O)。
3。プレフィックスを適用: 三酸化硫黄(3つの酸素原子を示しています)。
4。式を書きます: SO3
追加のヒント
* 練習は完璧になります! 書かれた式が多いほど、ルールで快適になります。
* 周期表を参照してください 要素の電気陰性度を判断するのに役立ちます。
* オンラインリソースを使用 例を見つけて問題を実践するための化学の教科書。
より多くの例をご覧になりたい場合はお知らせください!