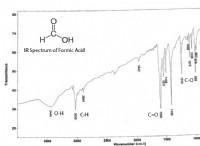
その理由は次のとおりです。
* 極性: カルボン酸基内のカルボニル基(C =O)は非常に極性であり、酸素原子に付着した水素原子を非常に酸性にしています。
* 電子撤退: カルボニル基の酸素原子は非常に電気陰性であり、O-H結合から電子密度を引き出します。これにより、結合が弱まり、水素がプロトン(H+)として放出される可能性が高くなります。
* 共鳴安定化: 水素イオンが放出されると、残りのカルボキシレートイオン(COO-)の負電荷は共鳴によって非局在化されます。この非局在化は、負電荷を安定させ、プロトンの放出をさらに有利にします。
したがって、カルボン酸基の存在により、有機分子は酸性になります。