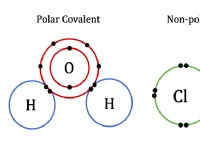
* 酸素の通常の酸化状態: 酸素はほとんど常に-2の酸化数を持っています。これは、酸素が非常に電気陰性であるため、化学結合で電子を自分自身に引き付ける傾向があるためです。
* カリウムの通常の酸化状態: カリウム(K)はグループ1要素であり、通常は酸化数+1です。
* バランス料金: Ko₃のようなニュートラル化合物では、酸化数の合計はゼロに等しくなければなりません。
可能性を分析しましょう:
*酸素の酸化数は+1/3であると仮定すると、カリウムの+1電荷のバランスをとるために3つの酸素原子が必要になります。 ただし、これにより、必要に応じて-1ではなく、酸素原子の合計+1が得られます。
* 正しい酸化状態: 電荷のバランスをとるには、KO₃の酸素の酸化状態は-2でなければなりません。これは、各酸素原子に-2電荷があることを意味し、合計-6を与えてくれます。 これのバランスをとるには、カリウムには+6の電荷が必要です。これは不可能です。
結論:
KO₃で+1/3酸化状態を持つ酸素の考え方を調整する方法はありません。式自体は安定した化合物を表していません。
可能性の高いシナリオ:
フォーミュラKO₃は間違っている可能性があります。 実際の化合物についてタイプミスや誤解に遭遇した可能性があります。