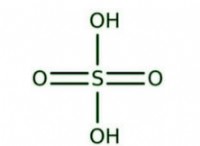
H2SO4:と反応するガス
* アンモニア(NH3): アンモニアは強い塩基であり、酸性H2SO4と反応して硫酸アンモニウム((NH4)2SO4)を形成します。
* アミン(RNH2、R2NH、R3N): アンモニアと同様に、アミンは塩基性であり、H2SO4と反応して塩を形成します。
* alkenes(c =c含有化合物): 濃縮されたH2SO4は脱水剤として作用することができ、アルケンの二重結合全体に加えて、アルキル硫酸塩の形成につながる可能性があります。
* アルキン(Cαを含む化合物): アルケンと同様に、アルキンは濃縮されたH2SO4と反応する可能性があります。
* エーテル(R-O-R): H2SO4はエーテルを切断し、C-O結合を破壊し、潜在的にアルコールとアルカンを形成することができます。
* アルコール(ROH): 濃縮されたH2SO4はアルコールを脱水し、アルケンと水を形成することができます。
重要な注意:
* H2SO4の反応性は濃度に依存します: 希釈H2SO4は上記のいくつかのガスと反応しないかもしれませんが、濃縮されたH2SO4ははるかに強力な脱水剤であり、より容易に反応する可能性があります。
代替乾燥剤:
これらのガスを乾燥させる必要がある場合は、代替乾燥剤の使用を検討してください。
* 塩化カルシウム(CACL2): あまり反応しないガスを含む多くのガスを乾燥させるのに適しています。
* 硫酸マグネシウム(MGSO4): 別の効果的な乾燥剤。
* 五酸化リン(P2O5): 乾燥ガスには非常に効果的ですが、水と非常に激しく反応します。
他のガスを念頭に置いているかどうかを教えてください。最良の乾燥方法を決定するのを手伝うことができます。