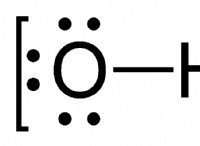* 電子の共有: 両方のタイプの結合には、2つの原子間で電子の共有が含まれます。 この共有は、共有結合の決定的な特徴です。
* 分子間力よりも強い: 両方のタイプの共有結合は、一般に、分子を一緒に保持する分子間力(水素結合や双極子双極子相互作用など)よりもはるかに強いです。これは、共有結合がより多くのエネルギーを壊す必要があることを意味します。
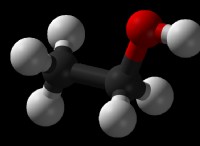
* 非金属間の形成: 通常、非金属原子間で極性結合と非極性共有結合の両方が発生します。
ただし、重要な違いは平等にあります 電子共有の:
* 非極性共有結合: 電子は等しく共有されます 原子間。これは、2つの原子が同じ電気陰性度(電子を引き付ける能力)を持っているときに発生します。
* 極性共有結合: 電子は不均等に共有されます 原子間。これは、1つの原子が他の原子よりも電気陰性度が高い場合に発生し、より多くの電気陰性原子の部分的な負電荷と、より少ない電気陰性原子での部分的な正電荷になります。
極性結合と非極性共有結合の違いは、厳格な部門ではなくスペクトルであることを理解することが重要です。 2つの原子間に電気陰性度の差が大きいほど、結合が極性になります。