水と混合する液体(混乱):
* アルコール: エタノール(飲酒アルコール)、メタノール、およびその他のアルコールは水と混和します。これは、それらが水分子と水素結合を形成するためです。
* 酢(酢酸): 酢の主要成分である酢酸は、水素結合を形成する能力のために水と混和します。
* グリセロール: 多くの製品で使用される濃厚で甘い液体であるグリセロールは、水素結合を形成できる複数のヒドロキシル基のおかげで水と混和します。
* アセトン: 一般的な溶媒であるアセトンは、水と弱い水素結合を形成し、混和性を発揮します。
* 多くの酸と塩基: 多くの酸と塩基は、水、特に非常に極性のあるものと混和しています。
なぜ一部の液体が水と混ざっているのか:
* 極性: 水は極性分子であり、つまり、わずかに正で、わずかに負の端があります。極性(アルコールなど)でもある液体は、正と負の電荷が互いに引き付けるため、水とよく混ざる傾向があります。
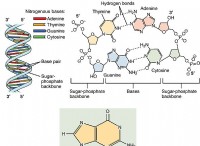
* 水素結合: 水は、酸素または窒素に結合した水素原子を持つ他の分子と強い水素結合を形成します。これが、多くのアルコールと酸が水と混ざり合っている主な理由です。
水と混ざっていない液体(不混意):
* オイル: オイルは非極性であり、水と水素結合を形成しません。これが、油と水が異なる層に分離する理由です。
* ガソリン: オイルと同様に、ガソリンは非極性であり、水と混ざりません。
* 水銀: 水銀は、室温で液体である金属です。水と混和することはなく、非常に有毒です。
重要な注意: 水と混ざるように見える可能性のある液体がいくつかありますが、実際には真の混合ではなく溶液を形成します。ソリューションは、コンポーネントが均等に分布する均質な混合物です。一方、真の混合物には、個々の特性を保持するコンポーネントがあります。
他に質問がある場合はお知らせください!