極性共有分子
* 水に溶ける: 極性の共有分子は、「同様の溶解のような」ルールのために、水によく溶解します。水は極性分子自体です。つまり、一方の端に部分的な正電荷、もう一方の端に部分的な負電荷があります。
* 例:
*砂糖(グルコースのような)
*エタノール(飲酒アルコール)
*酢酸(酢で見つかった)
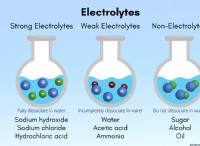
イオン分子
* 水に溶ける: イオン化合物は、正の帯電イオン(陽イオン)と負に帯電したイオン(アニオン)で構成されています。水の極性により、これらのイオンを囲み、分離し、イオン結合を破壊し、化合物を溶解できます。
* 例:
*テーブルソルト(NaCl)
*塩化カリウム(KCL)
*重炭酸ナトリウム(重曹)
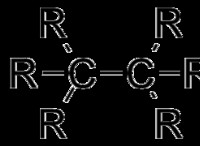
非極性分子
* 水によく溶解しないでください: 非極性分子には均一な電荷分布があります。つまり、有意な部分電荷はありません。彼らは水の極地分子と強く相互作用することができず、ほとんどが不溶性になります。
* 例:
*オイル(植物油のような)
*脂肪
*ガソリン
重要な概念
* 極性: 電気陰性度の違いによる分子内の不均一な電荷分布(電子を引き付ける原子の傾向)。
* 水素結合: 水分子は互いに強い水素結合を形成し、他の極性分子と溶解度に寄与します。
例外
「いいね」ルールは良い一般ガイドですが、常に例外があります。
* 一部の非極性分子は、水にわずかに溶解する可能性があります ファンデルワールスの力により、弱い形の魅力。
* 一部のイオン化合物はわずかに可溶性です イオン間の強い相互作用のため。
特定の例をより詳細に調べたい場合はお知らせください!