その理由は次のとおりです。
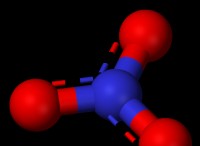
* 共有結合 原子間の電子の共有を伴います。この共有は、強力で比較的安定した結合を生み出し、定義された配置で原子をまとめます。
* イオン結合 、強力でもありますが、電子の伝達を伴い、イオン(荷電原子)の形成をもたらします。イオン化合物は異なるユニット(結晶格子のような)を形成できますが、配置は定義されていないため、通常は分子とは見なされません。
例外:
*一部の化学者は、NaCl(テーブルソルト)のような非常に小さく、密接に結合したイオン化合物も、その明確で明確に定義された構造のために分子と見なすことができると主張するかもしれません。
*特定の金属化合物は、共有結合特性を示すことができ、特殊なコンテキストで「分子」と呼ばれることもあります。
ただし、一般に、共有結合の存在は、分子を定義するための最も広く受け入れられている基準です。