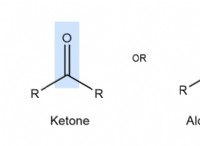
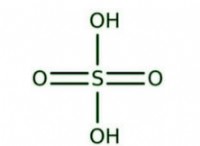
1。ルイス構造
* 炭素: 4価電子
* 水素: 1つの価電子それぞれ(合計2)
* 酸素: 6価電子
総価電子:4 + 2 + 6 =12
ルイス構造を描くには:
*炭素原子を中央に置きます。
* 2つの水素原子と酸素原子を炭素の周りに置きます。
*各原子を単一の結合(2つの共有電子を表す)で中央炭素に接続します。
* 2つの孤立した電子ペアを追加して、酸素原子のオクテットを完成させます。
ルイス構造:
o
||
H-C-H
2。共有電子のカウント
* C-H結合: 結合ごとに共有された2電子x 2結合=4電子
* c-o結合: 結合ごとに共有される2電子x 1結合=2電子
共有電子の合計:4 + 2 =6電子
したがって、ホルムアルデヒド(ch₂o)には6つの共有電子があります。