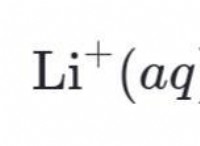その理由は次のとおりです。
* イオン化合物 は、反対に帯電したイオン(陽イオンと陰イオン)間の静電引力によって形成される化合物です。
* 二重変位反応 2つの反応物間のイオンの交換を伴います。
二重変位反応の一般的な形式:
AB + CD→AD + CB
どこ:
* AとCは陽イオンです
* bとdは陰イオンです
二重変位反応のタイプ:
1。降水反応: これらの反応により、可溶性イオン化合物を含む2つの溶液が混合されると、不溶性固体(沈殿)が形成されます。
例:
agno₃(aq) + naCl(aq)→agcl(s) +nano₃(aq)
2。中和反応: これらの反応は、酸とベースの間に発生し、塩と水を生成します。
例:
hcl(aq) + naoh(aq)→naCl(aq) +h₂o(l)
3。ガス進化反応: これらの反応は、製品の1つとしてガスを生成します。
例:
na₂co₃(aq) + 2hcl(aq)→2nacl(aq) +h₂o(l) +co₂(g)
重要な注意:
すべての二重変位反応は、イオン化合物を反応物として関与させますが、反応物が二重変位反応であるため、イオン化合物とのすべての反応はありません。たとえば、一部のイオン化合物は分解反応を起こし、より単純な物質に分解する可能性があります。