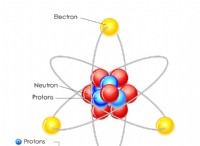
* 原子はニュートラルです: 原子には、自然に同数のプロトン(正の帯電した粒子)と電子(負に帯電した粒子)があります。このバランスは中立電荷をもたらします。
* イオン化: 原子が電子を失ったり獲得したりすると、イオンになります。
* cation: 原子が電子を失うと、陽イオンと呼ばれる正の帯電イオンになります。
* 2+電荷: 2+電荷は、原子が2つの電子を失っており、電子よりも2つの陽子が残っていることを示しています。
例:
マグネシウム原子(Mg)を考えてみましょう。 12個のプロトンと12個の電子があります。 2つの電子を失うと、マグネシウムイオン(mg²⁺)になります。現在、12個の陽子と10個の電子があり、+2の正味電荷が生じています。
キーポイント:
* イオン化は化学プロセスです: 他の原子または分子との相互作用のために発生する可能性があります。
* イオンの電荷は、失われたまたは得られた電子の数を反映しています: +2電荷は、原子が2つの電子を失ったことを意味します。
* イオンは化学反応において重要です: それらは、化学結合と化合物の形成において重要な役割を果たします。
特定のイオンに関する詳細情報やそれらの形成方法をお知らせください!