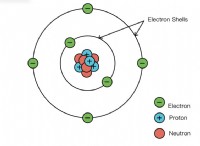
* ナトリウムイオンは正に帯電します。 彼らは電子を失い、+1電荷を与えました。
* 請求のように反発。 これは、2つのナトリウムイオンが、静電反発のために実際に互いに押しのけられることを意味します。
このように考えてみてください: 同じ極が向いている2つの磁石を想像してください。彼らは一緒に固執しません。彼らは撃退します。同じ原理がナトリウムイオンにも当てはまります。
ただし、:
* 溶液またはクリスタル: ナトリウムイオンは、塩化物イオン(Cl-)などの他のイオンと一緒に存在し、イオン結合を形成します。これらの結合は、反対に帯電したイオン間の強い静電魅力です。このシナリオでは、ナトリウムイオンは互いに隣人だけでなく、より大きな構造の一部になります。
* 特定の化学反応: 特定の条件下では、2つのナトリウムイオンが他の分子との化学反応に関与する可能性がありますが、これは反応に固有のものであり、隣の存在のためだけではありません。
要約: 2つのナトリウムイオンだけでは多くはありません。彼らはお互いを撃退するだけです。興味深い化学が起こる特定のコンテキストで他のイオンまたは分子と相互作用するときです。