* 極性: 水は極性分子であり、つまり、わずかに正の末端(水素原子)とわずかに陰性の末端(酸素原子)があります。この極性により、水分子は互いに強い水素結合を形成することができます。
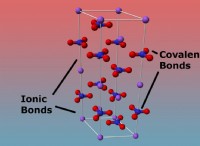
* 疎水性効果: 非極性分子は、非極性共有結合を持つものと同様に、この電荷分離を欠いており、水とうまく相互作用しません。彼らは水の水素結合ネットワークを破壊し、好ましくない相互作用につながります。 これが、疎水性と見なされる理由です 、「水恐怖」を意味します。
このように考えてみてください:
*油と水を混ぜようとすることを想像してください。非極性であるオイルは、水と混ざりません。これは、水分子が油分子よりもむしろお互いにくっつくためです。
例:
*脂肪と油には多くの非極性共有結合があり、疎水性になります。
*ワックスと炭化水素も非極性であるため、水が嫌いです。
重要な注意: 非極性分子は水に容易に溶けませんが、ヴァンデルワールス力と呼ばれる弱い一時的な相互作用を介して水と相互作用することができます。しかし、これらの力は、水素結合水分子が互いに形成されるよりもはるかに弱いです。