1。水の極性:
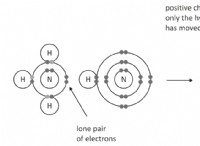
*水分子は極性です。これは、彼らがわずかに正の末端(水素側)とわずかに負の末端(酸素側)を持っていることを意味します。この極性により、水は他の極性分子またはイオンと強く相互作用することができます。
2。塩化ナトリウムのイオン性:
*塩化ナトリウムはイオン化合物です。正に帯電したナトリウムイオン(Na+)および負に帯電した塩化物イオン(CL-)で構成されています。これらのイオンは、強力な静電力によって結合されています。
3。水の溶解:
*塩化ナトリウムを水に加えると、極水分子はナトリウムイオンと塩化物イオンを囲みます。
*水分子の正の末端は負の塩化物イオンを引き付け、水分子の負の末端は陽性ナトリウムイオンを引き付けます。
*この引力は、イオンを固体NaClにまとめる静電力を克服し、イオンを水に分離して溶解します。
4。灯油の非極性の性質:
*灯油は非極性炭化水素です。 非極性分子には、水がある正と負の領域がありません。イオンとの強力な相互作用を形成する能力はありません。
5。塩化ナトリウムとの相互作用の欠如:
*灯油は非極性であるため、ナトリウムイオンと塩化物イオンを効果的に引き付けることはできません。 NaClでイオンを一緒に保持する静電力は強いままであり、化合物が溶解するのを防ぎます。
要約:
水の極性により、塩化ナトリウムのイオンと強く相互作用し、イオン結合を破壊し、溶解を引き起こすことができます。灯油の非極性性は、NaClの強いイオン力を克服するために必要な相互作用を形成することを防ぎます。