* 重曹はベースです: 重炭酸ナトリウムは弱い塩基です。水中では、部分的に解離して、重炭酸イオン(HCO3-)と水酸化物イオン(OH-)を形成し、pHを増加させます。
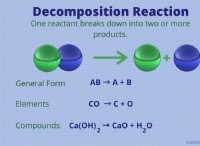
* 弱酸との反応: 重曹は、酢(酢酸)のような弱酸と反応して、塩、水、および二酸化炭素ガスを形成します。生成された塩は通常、元の酸よりも中性であり、pHの全体的な増加に寄与します。
例:
重曹を酢(酢酸)に加えると、次の反応が発生します。
NAHCO3(AQ) + CH3COOH(AQ)→CH3COONA(AQ) + H2O(L) + CO2(g)
* 重炭酸ナトリウム(NAHCO3) 酢酸(CH3COOH)と反応します 。
* 酢酸ナトリウム(CH3COONA) 形成されます。これは中性pHの塩です。
* 水(H2O) 生産されます。
* 二酸化炭素(CO2) ガスが放出され、多くの場合、泡立ちます。
この反応の正味の効果は、溶液の酸性度の低下であり、pH。の増加につながります。
重要なメモ:
* pH変化の程度は、酸の強度と重曹の量に依存します。
* 重曹を追加すると、溶液が基本的になりすぎる可能性があります。
* 化学物質、特に酸と塩基を混合するときは常に注意してください。