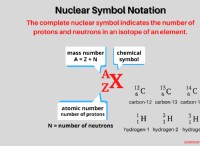
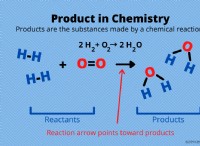
これがどのように機能しますか:
* イオン結合: ある原子から別の原子への電子の完全な移動があるときに発生し、互いに引き付ける反対に帯電したイオンが作成されます。これにより、原子間に大きな電気陰性度の違いが生じます。
* 共有結合: 原子が電子を共有して安定した電子構成を実現するときに発生します。これは、原子間の電気陰性度の違いが小さいときに起こります。
* 極性結合結合: これらの両極端の間に落ちます。電子の共有がありますが、共有は不平等です。これは、1つの原子が他の原子よりも高い電気陰性度を持っているためです。電気陰性度が高い原子は、共有電子をより強く引き付け、その原子に部分的な負電荷と他方に部分的な正電荷を生成します。
例: 水分子(H₂O)では、酸素原子は水素原子よりも電気陰性です。これにより、酸素原子の部分的な負電荷(Δ-)があり、水素原子に部分的な正電荷(Δ+)がある極性共有結合が生成されます。
キーテイクアウト: 結合の性質は、必ずしも厳密にイオン性または共有結合ではありません。 スペクトルがあり、多くの絆が両方の特性を示します。