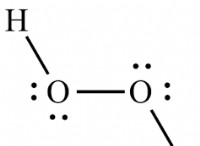
* 酸化数は電子に関するものであり、要素の基本性ではありません。 彼らは、すべての結合がイオン性である場合、原子が持つ電荷を説明しています。これは、化学反応における電子運動を追跡する方法です。
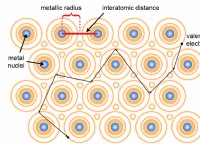
* 金属と非金属には異なる特性があります 、電子の構成と結合挙動に基づいています。
* 金属 安定した電子構成を実現するために、電子(正の酸化状態を形成)を失う傾向があります。
* 非金属 安定した電子構成を実現するために、電子(負の酸化状態を形成)を獲得する傾向があります。
ただし、いくつかの一般的な傾向があります:
* 金属 通常、陽性があります 酸化は化合物中に状態になりますが、特定の状況では陰性状態を持つことがあります。
* 非金属 通常、負のがあります 酸化状態ですが、特定の化合物に正の状態を持つことができるものもあります。
したがって、酸化数は手がかりになる可能性がありますが、要素が金属であるか非金属であるかの決定的な指標ではありません。
元素が金属であるか非金属であるかを判断するより良い方法は次のとおりです。
* 周期表の場所:
*金属は、周期表の左側にあります(遷移金属を含む)。
*非金属は、周期表の右側にあります。
* プロパティ:
* 金属: 光と電気の光沢のある、良い導体、順応性、延性。
* 非金属: 鈍い、貧弱な熱と電気の導体、脆い。
これらの一般的な傾向には例外があることを覚えておくことが重要です。金属(半金属)のようないくつかの要素は、金属と非金属の両方の特性を示します。