これが故障です:
* イオン結合: これらの結合は、有意に異なる電気陰性度の原子間に形成されます。 1つの原子(通常は金属)は電子を失い、正に帯電イオン(陽イオン)になり、もう1つの原子(通常は非金属)が電子をゲインし、負に帯電したイオン(アニオン)になります。 これらの反対に帯電したイオン間の静電引力は、化合物を一緒に保持します。 例には、テーブル塩(NaCl)と炭酸カルシウム(CACO3)が含まれます。
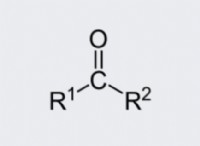
* 共有結合: これらの結合には、原子間の電子の共有が含まれます。この共有は、等しい(非極性共有結合)または不均等(極性共有結合)になります。 例には、水(H2O)と二酸化炭素(CO2)が含まれます。
イオン性結合と共有結合は無機化合物で最も一般的ですが、発生する可能性のある他の種類の結合があります。
* 金属結合: 電子が非局在化され、構造内のすべての原子の間で共有される金属に見られる。
* 共有結合結合: アンモニウムイオン(NH4+)のように、1つの原子が共有ペアに両方の電子を寄与します。
特に、より複雑な無機化合物に入ると、一部の化合物には異なる結合タイプの混合物が含まれている可能性があることに注意することが重要です。