その理由は次のとおりです。
* 弱い電解質: 過酸化水素は弱い電解質であり、溶液中に部分的にしかイオン化しないことを意味します。これは、電流を運ぶことができる多くの遊離イオン(荷電粒子)を生成しないことを意味します。
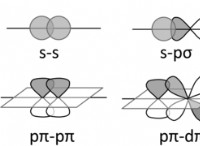
* 共有結合: 過酸化水素分子内の結合は共有結合であり、電子が原子間で共有されることを意味します。これにより、自由電子の動きが制限されます。これは、電気伝導率に不可欠です。
* 純粋なフォーム: 純粋な過酸化水素は、非極性分子であり、遊離イオンが存在しないため、導体が不十分です。
対照的に:
* 強い電解質: 強酸(塩酸など)または強い塩基(たとえば、水酸化ナトリウム)などの強力な電解質を含む溶液は、高濃度の遊離イオンを容易にイオン化して生成するため、良好な導体です。
* 金属: 金属は、簡単に移動して電流を運ぶことができる遊離電子の「海」が存在するため、電気の優れた導体です。
したがって、過酸化水素は非常に少量の電力を導入できますが、良好な導体とは見なされません。