* 電気陰性度: ナトリウムの電気陰性度は低く(0.93)、ヨウ素の電気陰性度が高くなっています(2.66)。これは、ヨウ素が電子のより強い魅力を持っていることを意味します。
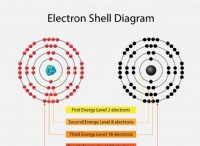
* 電子移動: ナトリウムとヨウ素が反応すると、ナトリウムは単一の原子価電子を失い、正に帯電したナトリウムイオン(Na+)になります。ヨウ素はこの電子を獲得して、負に帯電したヨウ化イオン(I-)になります。
* 静電引力: 反対に帯電したイオンは、静電力を通して互いに引き付けられ、イオン結合を形成します。
したがって、ヨウ化化合物ナトリウム(NAI)は、正に帯電したナトリウムイオンと負に帯電したヨウ化イオンの間の強力な静電誘引によってまとめられています。