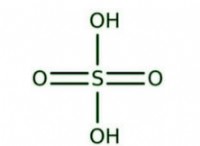
* 硫酸バリウム(baso₃)は、塩化バリウムと硫酸ナトリウムの反応によって形成されません。 これらの化合物は両方とも水に溶けますが、それらの反応は沈殿物を生成しません。
* 主な反応: 塩化バリウム(BACL₂)と硫酸ナトリウム(Na₂So₃)を溶液中に混合すると、二重変位反応が発生します。製品は硫酸バリウム(Baso₃)と塩化ナトリウム(NaCl)です。
bacl₂(aq) +na₂so₃(aq)→baso₃(s) + 2nacl(aq)
* 溶解度: 硫酸バリウムは水に控えめに溶けていますが、硫酸バリウムのように不溶性ではありません(baso₄)。これは、少量の硫酸バリウムが溶液に溶解することを意味し、著しい沈殿物の形成は見られません。
亜硫酸塩沈殿物を取得するには、別の反応が必要です:
* 亜硫酸イオン(亜硫酸ナトリウムなど)を含む溶液にバリウムイオンの供給源(塩化バリウムなど)を追加する。 しかし、それでも、硫酸バリウムの中程度の溶解度により、沈殿物は非常に最小限に抑えられます。
結論: 硫酸ナトリウムを含む溶液に塩化物イオンを添加しても、亜硫酸塩のバリウムは生成されません。