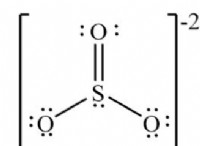
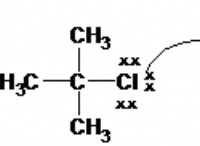
* 安定した構造: CO2の炭素原子は、両方の酸素原子と二重結合を形成し、非常に安定した線形構造をもたらします。 この強力な二重結合配置により、分子を分解することが困難です。
* 非極性分子: CO2は、その対称構造のため、非極性分子です。この極性の欠如は、酸塩基反応などの極性反応に関与する傾向を減らします。
* 弱いルイス酸: CO2は、電子ペアを受け入れることで弱いルイス酸として機能する可能性がありますが、この反応性はしばしば限られています。
ただし、CO2は、特に特定の条件下で、いくつかの反応に参加できます。
* 塩基との反応: CO2は、水酸化物(OH-)などの強力な塩基と容易に反応して炭酸塩を形成します。これは、CO2とLimewater(水酸化カルシウム溶液)の間の反応の基礎であり、CO2の検出に使用されます。
* 燃焼: 酸素と高温の存在下では、CO2をさらに酸化して一酸化炭素(CO)を形成できます。これは、燃焼プロセスにおける重要な反応です。
* 光合成: CO2は、光合成中の植物の炭素の主要な供給源です。植物は日光、水、CO2を利用してグルコースと酸素を生成します。
* 炭酸化: CO2は水に溶けて炭酸(H2CO3)を形成します。これは、炭酸飲料の寒い特性の原因となります。
* 特定の金属との反応: 高温では、CO2はマグネシウムなどの特定の金属と反応して金属酸化物と炭素を形成できます。
要約すると、二酸化炭素は一般的に反応性がありませんが、特に塩基、高温、または触媒の存在下で、特定の条件下でその反応性を高めることができます。