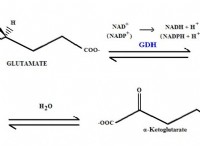
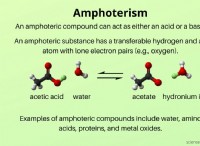
主な違い - アルキル化とアシル化
アルキル化は、アルキル化剤を使用して、ある分子から別の分子にアルキル基を移動させることです。これらのアルキル化剤 目的の脂肪族炭化水素鎖を出発物質に追加する能力があります。 アルキル化とは異なり、アシル化はアシル化剤を使用してアシル基を化合物に付加するプロセスです。これらのアシル化剤 必要な RCO- グループを開始材料に追加する機能があります。 これが主な違いです アルキル化とアシル化の間。
アルキル化とは
アルキル化は、出発物質に炭化水素鎖を導入するプロセスです。炭化水素は、炭素原子と水素原子で構成される最も一般的なタイプの有機化合物です。出発原料への 1 つの炭素原子 (メチル基) の付加は、メチル化として知られています。
アルキル基は、アルキルカルボカチオン、フリーラジカル、カルボアニオン、またはカルビンとして転移できます。したがって、アルキル化剤は、求電子性と求核性に基づいて、主に 2 つのカテゴリーに分けることができます。求核性アルキル化剤は、反応中にアルキルアニオン(カルバニオン)を形成し、カルボニル基などの電子不足炭素原子を攻撃します。 (例:グリニャール、有機リチウム、有機銅、有機ナトリウム試薬)。求電子アルキル化剤は、反応中にアルキルカチオン(カルボカチオン)を形成します(例:アルキルヘリド)。次の反応は、ベンゼンのフリーデルクラフツ アルキル化のメカニズムを示しています。
ステップ 1: ハロゲン化アルキルはルイス酸と反応して、より多くの求電子性炭素を生成します。 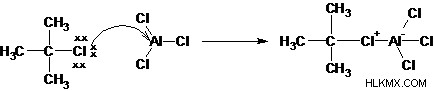
ステップ 2: ハロゲン化物の除去により、アルキルカルボカチオンが作成されます。
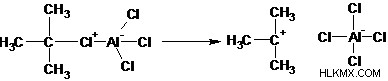
ステップ 3: 芳香環のπ電子は求核剤として作用し、芳香族性を失いながらカルボカチオンを攻撃します。 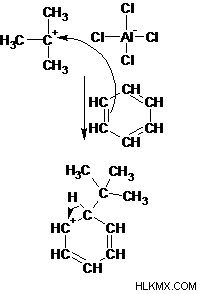
ステップ 4: プロトンの除去は芳香族系を再生します
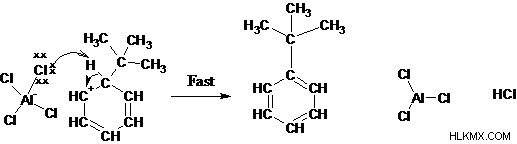
アシル化とは
アシル化は、アシル化剤を使用して出発物質にアシル基を付加するプロセスです。アシル基は、RCO の分子式を持つ官能基です。
アシル化剤は、金属触媒で処理すると強力な求電子剤を形成し、容易に求電子置換を受けます。ハロゲン化アシルは、最も一般的に使用されるアシル化剤であり、求電子置換によってケトンを生成します。さらに、カルボン酸のハロゲン化アシルおよび無水物は、求核置換によってアミンおよびアルコールをアシル化するためのアシル化剤として使用される。次の反応は、ベンゼンのフリーデルクラフト アシル化のメカニズムを示しています。
ステップ 1: ハロゲン化アシルはルイス酸と反応して錯体を形成します。 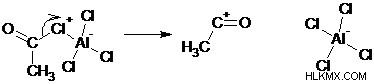
ステップ 2: ハロゲン化アシルからハロゲン化物が失われると、求電子性アシリウム イオンが生成されます。

ステップ 3: ベンゼンのπ電子は求核剤として働き、求電子性アシリウムイオンを攻撃します。この段階で芳香族性が破壊され、シクロヘキサジエニルカチオン中間体が得られます。 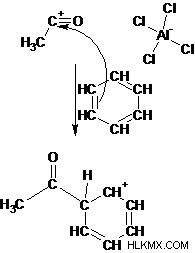
ステップ 4: プロトンの除去により、芳香族系と活性触媒が再生されます。 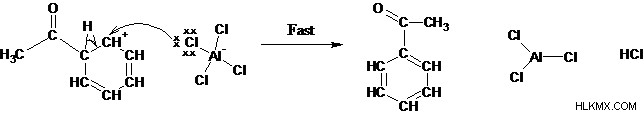
アルキル化とアシル化の違い
定義
アルキル化 :アルキル化は、出発物質に炭化水素鎖を導入するプロセスです。
アシル化 :アシル化は、アシル化剤を使用して出発物質にアシル基を付加するプロセスです。
全体的な変化
アルキル化: 全体的な変換は R-H から R-R’ です。
アシル化: 全体的な変換は、R-H から R-COR へです。
試薬
アルキル化: 一般に、ハロゲン化アルキル (すなわち R-Cl) および三塩化アルミニウム (すなわち AlCl
アシル化: 一般に、ハロゲン化アシル (すなわち R-COCl) および三塩化アルミニウムなどのルイス触媒が試薬として機能します。あるいは、酸無水物、すなわち (RCO)2 O はハロゲン化アシルの代わりに使用できます。
求電子種
アルキル化: カルボカチオン (i.e. R ) は、ルイス酸触媒によるハロゲン化物の「除去」によって形成されます。
アシル化: アシル カチオンまたは アシリウム イオン (つまり. RCO ) は、ルイス酸触媒によるハロゲン化物の「除去」によって形成されます。
カルボカチオンの再配置
アルキル化: カルボカチオンは転位しやすく、非常に安定したカルボカチオンを形成し、アルキル化反応が起こります。
アシル化: アシリウムイオンは共鳴構造により安定化される。この追加の安定性により、カルボカチオンの再配置が防止されます。
フリーデルクラフト反応
アルキル化: ハロゲン化ビニルまたはハロゲン化アリールは、中間体のカルボカチオンが不安定なため、アルキル化反応を受けません。
アシル化: HCOCl は反応条件下で CO と HCl に分解されるため、アシル化反応では常にケトンが生成されます。