化学結合としても知られる一次結合 、最も強いタイプの結合です 化学。それらは、原子を一緒に保持して分子を形成する責任があり、原子間の電子の共有または伝達によって特徴付けられます。これらの結合は、原子の正に帯電した核と負に帯電した電子の間の静電相互作用から生じます。
主要な債券には3つの主要なタイプがあります。
1。イオン結合:
* 完全な転送を通じて形成 ある原子から別の原子への電子の。
* イオンの形成をもたらします 反対の料金で。
*反対に帯電したイオン間の静電魅力はそれらをまとめます。
*例:NaCl(テーブルソルト)、MGO(酸化マグネシウム)
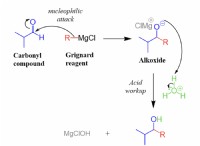
2。共有結合:
* 共有を通じて形成 2つの原子間の電子の。
*極地にすることができます (不平等な共有、部分的な料金をもたらす)または非極性 (平等な共有、ネット料金なし)。
*例:H₂O(水)、CO₂(二酸化炭素)、Ch₄(メタン)
3。金属債:
*電子が非局在化されている金属で見つかった 金属格子全体で自由に移動できます。
*この電子の非局在化は、正に帯電した金属イオンと負に帯電した電子海との間に強い魅力を生み出します。
*これは、金属の高い電気的および熱伝導性、延性、柔軟性を説明しています。
*例:金(au)、銅(cu)、銀(ag)
一次結合を理解することは重要です:
* 分子構造の予測: 原子結合を理解することは、分子の形状と形状を予測するのに役立ちます。
* 化学的特性の説明: 一次結合は、融点、沸点、溶解度、反応性など、物質の特性の多くを決定します。
* 化学反応の理解: 化学反応には、化学結合の破壊と形成が含まれます。
一次結合を超えて:
一次結合は最強ですが、二次結合もあります 、水素結合やファンデルワールスの力のように、物質の特性に影響を与える可能性があります。これらの力は弱いですが、分子間の相互作用に重要な役割を果たします。
要約:
一次結合は化学の基礎であり、原子をまとめて分子を形成します。彼らの性質とタイプを理解することは、物質の構造と行動を理解するために重要です。