その理由は次のとおりです。
* 共有結合は強い: 共有結合は、原子間の電子の共有によって形成されます。これらの結合は非常に強く、壊れるのにかなりの量のエネルギーが必要です。
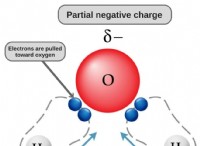
* 水の役割: 水は極性溶媒です。つまり、正と負の端があります。分子固体が水に溶けると、水分子は分子間力を介して固体の個々の分子と相互作用します 、水素結合や双極子双極子相互作用など。
* 溶解と破壊債: 溶解するには、分子が互いに分離されますが、それらの分子内の共有結合の破壊は含まれません。
例:
砂糖が水に溶けることを考えてください。砂糖分子は、共有結合によってまとめられています。砂糖が溶けると、水分子は糖分子を囲み、砂糖分子を固体状態で一緒に保持する分子間力(水素結合など)を壊します。ただし、糖分子内の共有結合はそのままのままです。
例外:
この一般的なルールにはいくつかの例外があります。
* 加水分解: 場合によっては、水は共有結合を破る化学反応に関与する可能性があります。このプロセスは加水分解と呼ばれます。
* 非常に反応性分子: 一部の分子固体には、水と反応する可能性のある非常に反応性のあるグループが含まれている可能性があり、潜在的に共有結合を破壊する可能性があります。
ただし、ほとんどの場合、分子固体が水と混合すると、分子内の共有結合はそのままのままです。