* 非金属 電気陰性度が高い傾向があります。つまり、電子に強い魅力があります。また、酸素と結合する場合、これも非常に感動的であるため、電気陰性度の違いはイオン結合を形成するほど大きくありません。
* 共有結合 原子が電子を共有するときに形を形成します。非金属酸化物では、非金属および酸素原子が電子を共有して、安定したオクテット構成を実現します。
非金属酸化物の例:
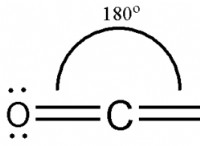
*二酸化炭素(co₂)
*二酸化硫黄(so₂)
*二酸化窒素(いいえ)
*水(h₂o)
例外:
この規則には、特に複数の酸化状態を形成できる金属では、いくつかの例外があります。たとえば、一部の遷移金属は、マンガン(VII)酸化物(Mn₂O₇)のように、イオン性と見なされる酸化物を形成できます。ただし、一般に、非金属酸化物は共有結合です。