金属と酸のシンボル方程式:
金属と酸との反応の一般的なシンボル方程式は次のとおりです。
金属 +酸→塩 +水素ガス
例:
* マグネシウム +塩酸→塩化マグネシウム +水素ガス
シンボル方程式:
mg(s) + 2hcl(aq)→mgcl₂(aq) +h₂(g)
説明:
* 金属: 金属は、その化学記号(マグネシウムのmgなど)で表されます。
* 酸: 酸は、その化学式(たとえば、塩酸のHCl)で表されます。
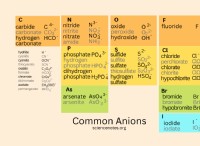
* 塩: 塩は、酸から金属陽イオン(陽イオン)と陰イオン(負イオン)によって形成されます。塩の化学式は、イオンの電荷のバランスをとることによって決定されます(例えば、塩化マグネシウムのMgcl₂)。
* 水素ガス: 水素ガスは、反応の副産物として生成されます。化学式H₂で表されます。
注: すべての金属がすべての酸と反応するわけではありません。酸との金属の反応性は、反応性シリーズの金属の位置に依存します。反応性シリーズで高く金属が酸とより容易に反応します。
他の金属酸反応の例:
* 亜鉛 +硫酸→硫酸亜鉛 +水素ガス
* zn(s) +h₂so₄(aq)→znso₄(aq) +h₂(g)
* 鉄 +塩酸→鉄(II)塩化物 +水素ガス
* fe(s) + 2hcl(aq)→fecl₂(aq) +h₂(g)
この一般的な方程式と例は、この反応の重要な特性を強調し、塩と水素ガスの形成を示しています。