その理由は次のとおりです。
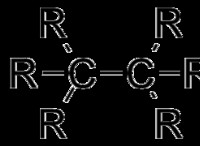
* Valence Shell: 原子の最も外側のシェルは、価数シェルと呼ばれます。化学結合に関与する電子が含まれています。
* 完全な価数シェル: 完全な価数シェルは、一般に8つの電子を持つと見なされます(最大2つの電子を持つ最初のシェルを除く)。この構成により、原子が安定し、反応性が低下します。
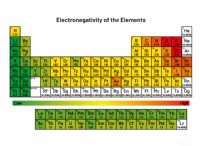
* メタロイド: 金属は、金属と非金属の両方の特性を示す要素です。それらは、周期表の金属から金属を分離する「階段」ラインに沿って位置しています。それらは金属と非金属の間にあるユニークな電子構造を持っているため、それらは部分的に満たされた原子価殻を持っています 。
したがって、メタロイドには、価数貝殻に中間数の電子があり、完全なシェルを持つ元素よりも安定性が低くなりますが、少数の原子価電子のみを持つ元素ほど反応性はありません。