1。 還元剤としてのナトリウム:
* 一般原則: ナトリウムは非常に反応性のある金属であり、その電子を容易に放棄してナトリウムイオン(Na+)になります。これにより、強力な還元剤になります。つまり、他の種に電子を供給し、電子を獲得します(還元されます)。
* 有機化学への応用: ナトリウムが特定の有機化合物と反応すると、カルボニル基(C =O)やハロゲン(CL、BR、I)などの官能基に電子を供給できます。これにより、これらの機能グループが減少します。
2。 特定の反応と例:
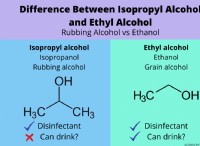
* アルコールとの反応: ナトリウムはアルコール(エタノールなど)と激しく反応して、アルコキシドと水素ガスを形成します。
* 2roH + 2NA→2RONA +H₂
* カルボン酸との反応: ナトリウムはカルボン酸と反応してカルボン酸塩と水素ガスを形成します。
* 2RCOOH + 2NA→2RCOONA +H₂
* wurtz反応: ナトリウムは、アルカンを形成するためにハロゲン化アルキルを結合する方法であるWurtz反応において重要です。
* 2RX + 2NA→R-R + 2NAX(Rはアルキル基であり、Xはハロゲンです)
3。 安全上の考慮事項:
* 発熱反応: ナトリウムと有機化合物との反応はしばしば発熱性であり、熱を放出します。制御されていない反応や潜在的な爆発を避けるために注意する必要があります。
* ナトリウムの取り扱い: ナトリウムは危険な材料であり、水で激しく反応します。適切な安全装置と手順を使用して、注意して処理する必要があります。
4。 アプリケーション:
* 新しい化合物の合成: ナトリウムと有機化合物の反応は、アルコール、アルデヒド、ケトン、アルカンなど、さまざまな有機化合物の合成に使用されます。
* 分析化学: ナトリウム還元を使用して、有機分子の官能基を特定できます。
要約:
ナトリウムの強力な還元力は、有機化学の有用な試薬となります。官能基を減らし、新しい化合物を合成し、Wurtz反応のような特定の反応に重要な反応に関与します。 その反応性には慎重な取り扱いが必要であるため、ナトリウムを使用するときは常に安全性を優先します。